- Умный справочник
- Химия
- Карбоновые кислоты
Карбоновые кислоты
Карбоновые кислоты — органические соединения, содержащие группу -COOH.
Молекулярная формула — CnH2nO2.
Eсли нужно найти молекулярную формулу пропановой кислоты, в которой 3 углерода, то получаем C₃H₂x₃O₂ → C₃H₆O₂.
- Низкомолекулярные кислоты — жидкости
- Насыщенные высокомолекулярные (жирные) кислоты — твердые
- Ненасыщенные высокомолекулярные кислоты — жидкие
Приятного изучения статьи! Если хочешь подготовиться на 90+, то обязательно посмотри вот эти способы подготовки (жми, чтобы перейти на сайт и узнать подробнее) 💜
Номенклатура
Систематически карбоновые кислоты и их соли называются следующим образом.
HCOOH — метановая кислота, соли — метаноаты
CH₃-COOH — этановая кислота, соли — этаноаты
CH₃-CH₂-COOH — пропановая кислота, соли — пропаноаты
HOOC-COOH — этандиовая кислота, соли – этандиоаты
Но для кислот намного более распространенными являются тривиальные названия, они есть в статье по тривиальным названиям в органике.
HCOOH — муравьиная кислота, соли — формиаты
CH₃-COOH — уксусная кислота, соли — ацетаты
CH₃-CH₂-COOH — пропионовая кислота, соли — пропионаты
HOOC-COOH — щавелевая кислота, соли — оксалаты
Производные карбоновых кислот
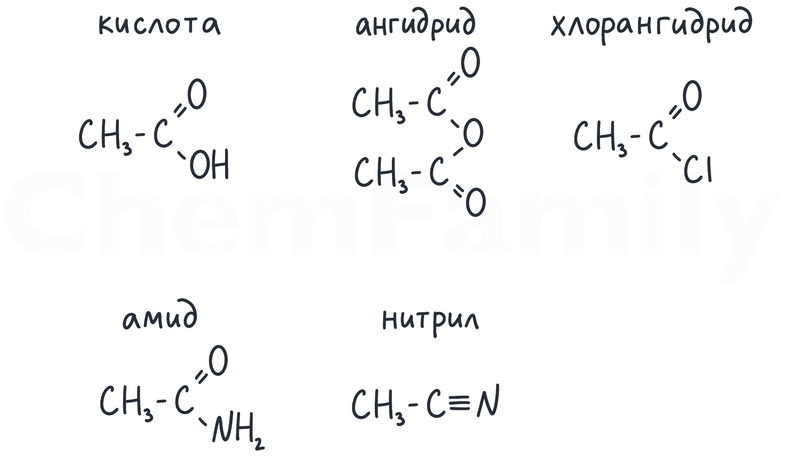
Общие свойства кислот
Карбоновые кислоты вступают во все типичные для кислот реакции. Они взаимодействуют с металлами левее водорода в ряду активности металлов, с основными и амфотерными оксидами, гидроксидами.
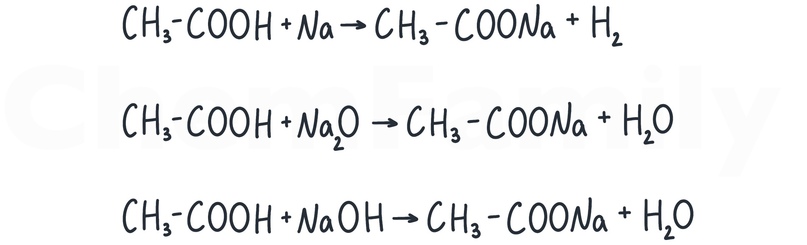
Отдельно стоит отметить соли, с которыми есть взаимодействие: карбонаты, гидрокарбонаты, сульфиты, гидросульфиты.
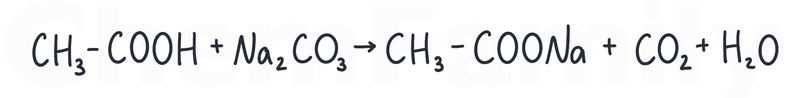
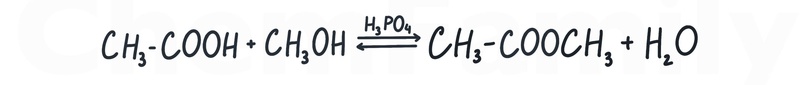
Образование сложных эфиров
При взаимодействии спирта и кислоты образуется сложный эфир. Реакция идет в кислой среде (лучше взять H₃PO₄) и обратима.
Название сложного эфира складывается из названия спирта и кислоты. Так, эфир CH₃COOCH₃, образованный уксусной кислотой и метанолом, будет называться метилацетат. А эфир HCOOC₂H₅, образованный муравьиной кислотой и этанолом, будет называться этилформиатом.
Водный гидролиз сложных эфиров
Гидролиз — расщепление с помощью воды. При водном гидролизе сложные эфиры распадаются на то, из чего образовались, то есть на кислоту и спирт. Реакция идет в кислой среде, лучше использовать H₃PO₄. Реакция обратима.
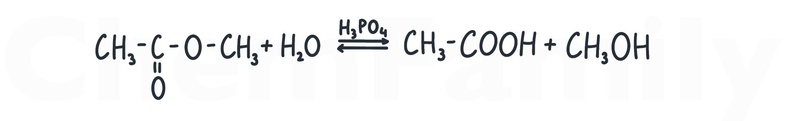
Если в качестве среды взята HCl, то образовавшийся спирт с ней взаимодействовать не будет, так как для этой реакции нужны более жесткие условия.
Щелочной гидролиз сложных эфиров
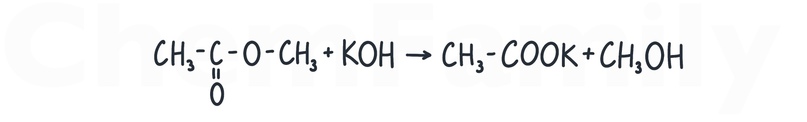
Щелочной гидролиз идет в щелочной среде, поэтому образуется не кислота, а ее соль, и реакция становится необратимой.
Альфа-хлорирование кислот
При добавлении хлора в присутствии красного фосфора хлор встает к ближайшему к группе -COOH углероду (альфа-положение).
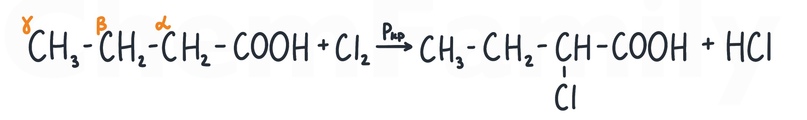
Особые свойства муравьиной кислоты
Муравьиная кислота обладает уникальными свойствами — в ней есть одновременно и альдегидная, и кислотная группа.
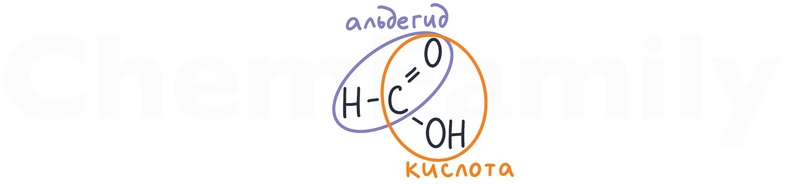
Поэтому это единственная кислота, которая может вступать в реакцию серебряного зеркала. При этом она окисляется до CO₂, который тут же взаимодействует с NH₃, и образуется (NH₄)₂CO₃.
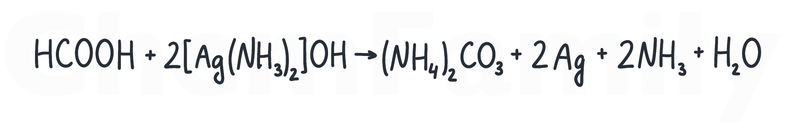
Остальные карбоновые кислоты тоже могут взаимодействовать с гидроксидом диамминсеребра(I). Но это будет реакция по типу «кислота+основание», а не реакция серебряного зеркала.
Гидроксидом меди(II) муравьиная кислота тоже окисляется.
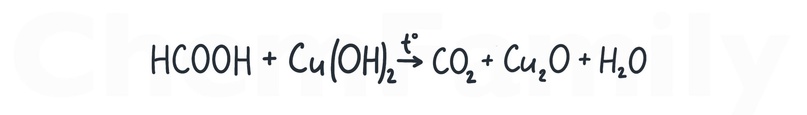
Получение кислот из тригалогеналканов
Три группы -OH, находящиеся у одного атома углерода, являются неустойчивой структурой, которая отщепляет молекулу H₂O и превращается в кислоту. Но так как реакция идет в щелочной среде, лучше написать соль.
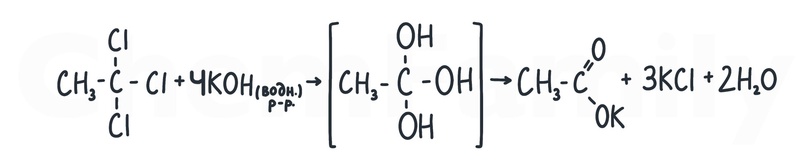
Взаимодействие NaOH с CO
Хоть CO и является несолеобразующим оксидом, но при взаимодействии с твердой щелочью образуется соль муравьиной кислоты.
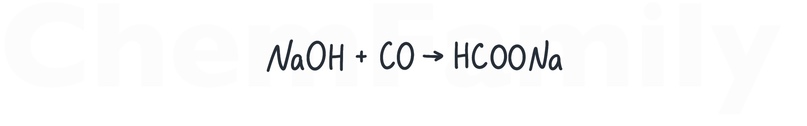
Декарбоксилирование солей карбоновых кислот (реакция Дюма)
Сплавление соли карбоновой кислоты с твердой щелочью.
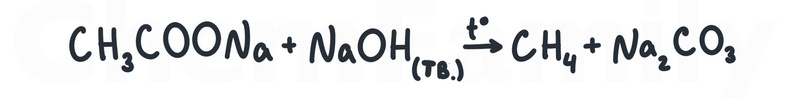
Сжигание солей карбоновых кислот
Эта реакция часто встречается в органической задаче из второй части.
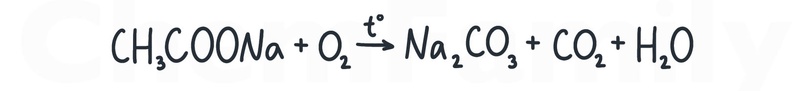
неФИПИшные реакции
Дальше идут реакции, которые в ЕГЭ не попадались (неФИПИшные), но попадались в разных авторских сборниках для подготовки. Их можно выучить, но не в первую очередь. И во второй части я бы их не писал, если есть аналогичные ФИПИшные реакции.
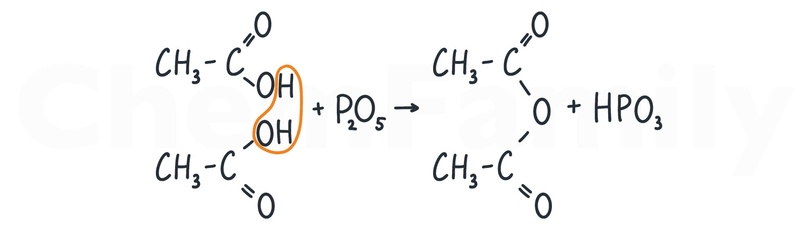
Получение ангидридов кислот
Ангидриды — производные кислот. Для их получения нужно добавить P₂O₅, который отщепит молекулу H₂O.
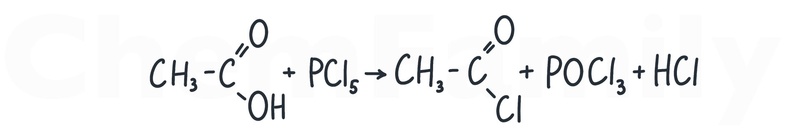
Получение хлорангидридов кислот
Хлорангидриды — производные кислот.
Получение амидов кислот
Амиды — производные кислот. Образуются при взаимодействии хлорангидрида и аммиака.
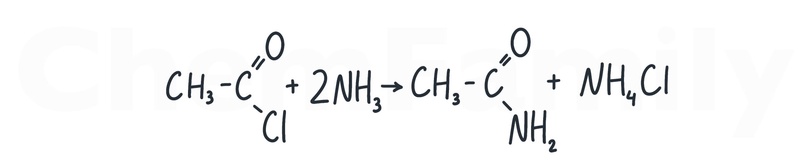
Получение нитрилов из амидов
Для получения нитрила от амида нужно отнять молекулу H₂O с помощью P₂O₅.
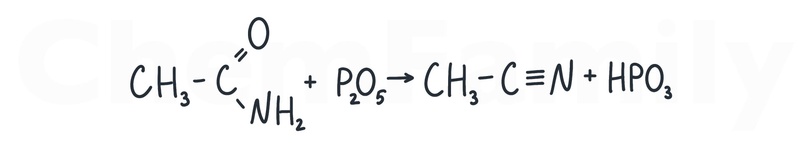
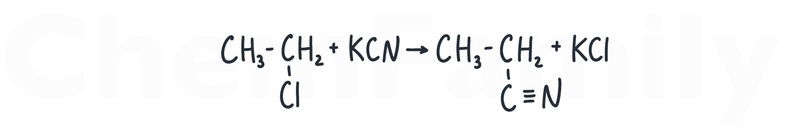
Получение нитрилов из галогеналканов
Нитрилы — производные карбоновых кислот. Для их получения нужно добавить к галогеналкану цианид щелочного (Li, Na, K, Rb, Cs, Fr) металла.
Взаимодействие нитрилов с водой
При взаимодействии с водой нитрилы образуют соли аммония.

