- Умный справочник
- Химия
- Альдегиды/кетоны
Альдегиды/кетоны
Альдегиды — органические вещества, содержащие альдегидную группу.
Кетоны — органические вещества, содержащие кето-группу.
Хотя альдегиды и кетоны имеют несколько разные свойства, они относятся к одному классу веществ, поскольку альдегидная группа это та же самая кето-группа, у которой вместо одного из радикалов стоит H.

Приятного изучения статьи! Если хочешь подготовиться на 90+, то обязательно посмотри вот эти способы подготовки (жми, чтобы перейти на сайт и узнать подробнее) 💜
Номенклатура
Чтобы получить название альдегида, надо прибавить к показывающему количество углеродов корню -аль.
CH₃-CH₂-CHO — 3 углерода → пропан + -аль = пропаналь.
Чтобы получить название кетона, надо прибавить к показывающему количество углеродов корню -он + указать положение кето-группы.
CH₃-C(O)-CH₂-CH₂-CH₃ — 5 углеродов → пентан + -он + 2 = пентанон-2.
Молекулярная формула альдегидов/кетонов — C𝑛H2𝑛O.
Если нужно найти молекулярную формулу этаналя, в котором 2 углерода, то получаем C₂H₂x₂O → C₂H₄O.
Альдегиды/кетоны с углеродным скелетом до примерно С12 — жидкости. Далее — твердые вещества.
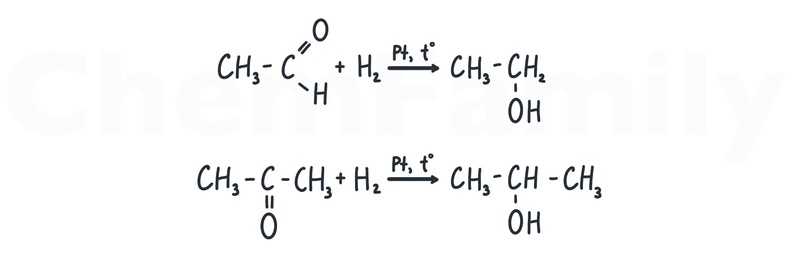
Гидрирование
В качестве катализатора лучше использовать Pt. Еще можно LiAlH₄, но он в ЕГЭ давно не попадался.
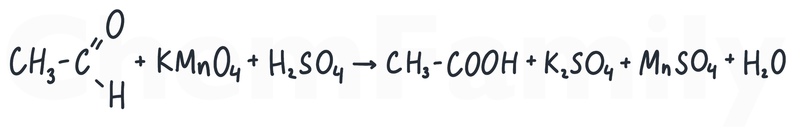
Окисление альдегидов до кислот с помощью KMnO₄
В качестве окислителя можно использовать любой раствор KMnO₄ или кислый раствор K₂Cr₂O₇.
При окислении водным раствором KMnO₄ побочными продуктами будут MnO₂ и KOH
При окислении щелочным раствором KMnO₄ – K₂MnO₄ и H₂O
При окислении подкисленным серной кислотой раствором K₂Cr₂O₇ – Cr₂(SO₄)₃, K₂SO₄ и H₂O
При окислении в нейтральной/щелочной среде образутеся не кислота, а соль!
Реакция серебряного зеркала
Во второй части важно записывать аммиачный раствор оксида серебра(I) именно так.
Аммиачный раствор оксида серебра (I), он же гидроксид диамминсеребра(I), он же реактив Толленса.
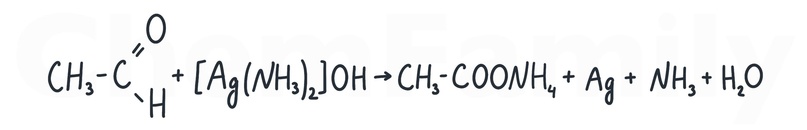
Окисление альдегидов до кислот с помощью Cu(OH)₂
Без нагревания образуется желтый CuOH. При нагревании CuOH распадается до красного Cu₂O.
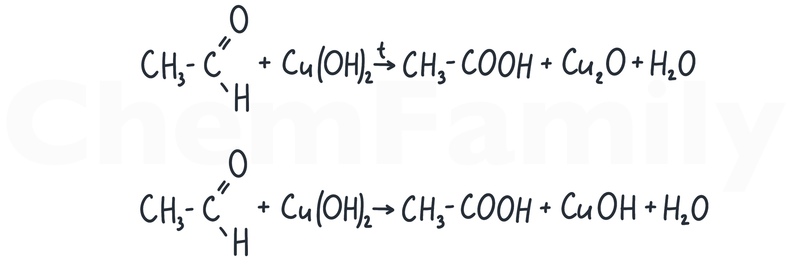
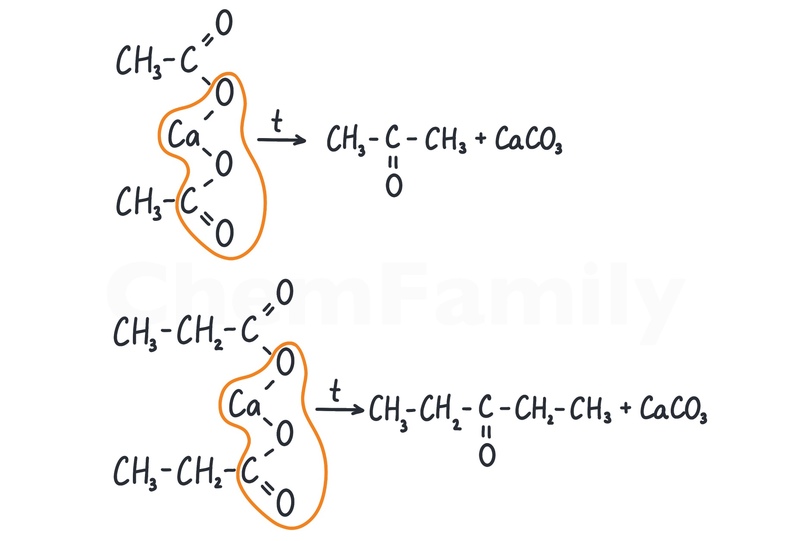
Термическое разложение солей карбоновых кислот
Вместо солей кальция можно использовать соли бария.
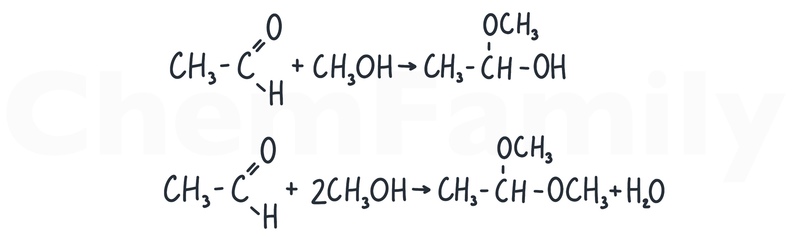
Взаимодействие альдегидов со спиртами
При взаимодействии с одной молекулой спирта образуется полуацеталь, а с двумя молекулами спирта — ацеталь. Во второй части эта реакция не попадалсь, но в первой части она встречается.
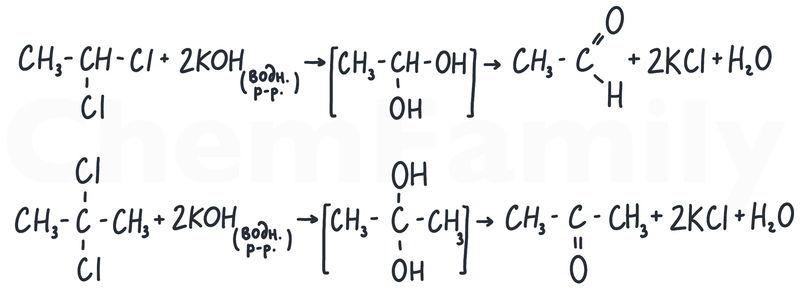
Получение альдегидов из дигалогеналканов
Две группы -OH, находящиеся у одного атома углерода, являются неустойчивой структурой, которая отщепляет молекулу H₂O и превращается в альдегид или кетон.
неФИПИшные реакции
Дальше идут реакции, которые в ЕГЭ не попадались (неФИПИшные), но попадались в разных авторских сборниках для подготовки. Их можно выучить, но не в первую очередь. И во второй части я бы их не писал, если есть аналогичные ФИПИшные реакции.
Взаимодействие с HCN

Окисление альдегидов бромной водой
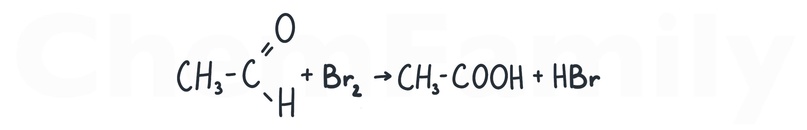
Хлорирование с помощью PCl₅

Гидратная форма
В растворе альдегиды в некоторой степени реагируют с водой, образуя гидратные формы. Формальдегид в растворе практически на 100% представлен гидратной формой но ацетальдегид уже значительно в меньшей степени.
