- Умный справочник
- Химия
- Алкены
Алкены
Алкены — углеводороды, в которых есть 1 двойная связь.
Молекулярная формула алкенов CnH2n.
Если нужно найти молекулярную формулу гептена, в котором 7 углеродов, то получаем C₇H₂x₇ → C₇H₁₄.
Низкомолекулярные алкены (С₁-С₄) — газы. С увеличением количества углеродов алкены становятся жидкостями, а потом твердыми веществами.
За счет двойной связи алкены являются более реакционноспособными, чем алканы. Интуитивно кажется, что двойная связь является более прочной, чем одинарная, однако это не так. Дело в том, что двойная связь состоит из одной прочной σ-связи и одной непрочной π-связи, которая и рвется в реакциях.
Приятного изучения статьи! Если хочешь подготовиться на 90+, то обязательно посмотри вот эти способы подготовки (жми, чтобы перейти на сайт и узнать подробнее) 💜
Галогенирование алкенов
С алкенами способны взаимодействовать все галогены: фтор, хлор, бром и йод.
Галогенирование идет с разрывом двойной связи и присоединением галогена к месту разрыва.
Для бромирования можно использовать как газообразный бром, так и бромную воду.
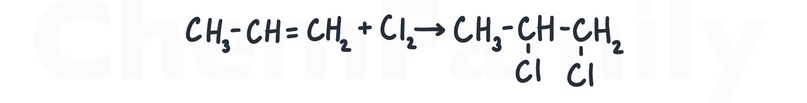
Гидрогалогенирование алкенов
Гидрогалогенирование — присоединение галогеноводорода, то есть HF, HCl, HBr или HI.
С симметричными алкенами все просто:
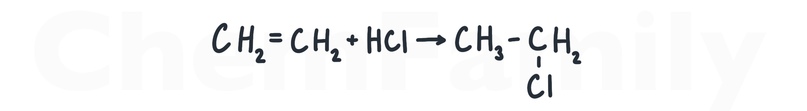
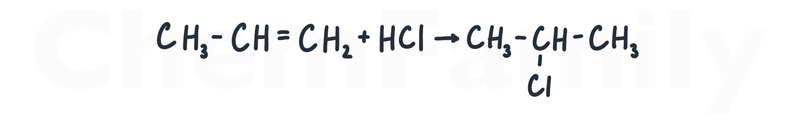
В несимметричном алкене надо решить, куда пойдет водород, а куда галоген. Это определяется правилом Марковникова — водород идет к тому углероду при двойной связи, где больше водородов, а галоген к оставшемуся углероду.
Гидрогалогенирование алкенов против правила Марковникова
Реакцию можно провести и против правила Марковникова, если использовать в качестве катализатора перекись водорода (H₂O₂). Лучше всего тут писать именно гидробромирование, потому что насчет протекания этой реакции с другими галогеноводородами есть вопросы.
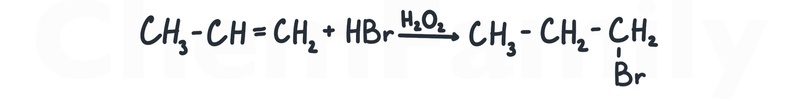
В настоящей неЕГЭшной химии нужно хорошо разбираться в механизмах протекания органических реакций, потому что в зависимости от структуры молекулы реакция может пойти не совсем так, как должна была. В ЕГЭ встречалась только одна реакция, в которой из-за индуктивного эффекта гидрогалогенирование шло против правила Марковникова.
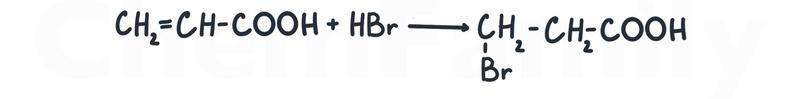
В гидрогалогенировании алкенов первым к молекуле присоединяется H⁺. Кислороды в карбоксильной группе имеют высокую электроотрицательность и перетягивают электронную плотность в связи C=C в свою сторону (это и есть индуктивный эффект). Таким образом, правый углерод в связи C=C становится более отрицательным, чем левый. Поэтому к правому более отрицательному углероду присоединяется H⁺, а Hal⁻ идет тогда к оставшемуся левому более положительному углероду.
Гидратация алкенов
Гидратация, то есть добавление воды, протекает в кислой среде, поэтому над стрелкой нужно написать какую-нибудь кислоту в качестве катализатора — лучше всего H₃PO₄, т.к. она создает кислую среду, но не взаимодействует с органическим веществом.
Если присоединение идет к несимметричному алкену, то нужно снова использовать правило Марковникова.
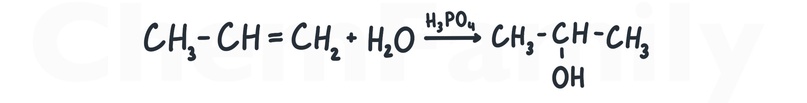
Гидрирование алкенов
Для гидрирования, присоединения водорода, нужно использовать один из трех катализаторов — Pt, Pd, Ni.
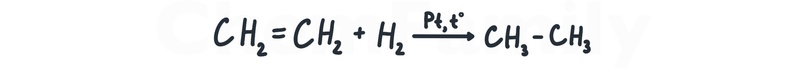
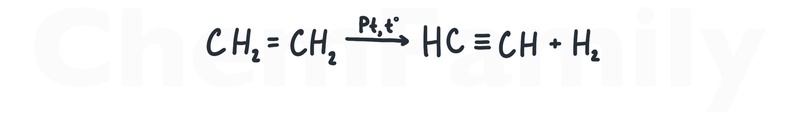
Дегидрирование алкенов
И для гидрирования, и для дегидрирования, применяется один из тех же трех катализаторов: Pt, Pd или Ni.
Мягкое окисление алкенов
Мягкое окисление протекает в присутствии водного раствора KMnO₄ при 0⁰С (реакция Вагнера).
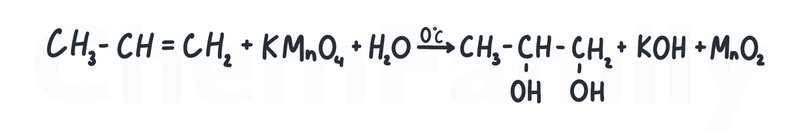
Насчет окисления щелочным раствором KMnO₄ мнения разнятся. Где-то пишут, что будет мягкое окисление с получением спирта с двумя группами OH-. Где-то пишут, что будет жесткое окисление (см. след раздел). В официальных заданиях окисление алкенов щелочным раствором KMnO₄ не попадалось. Поэтому лучше держать в голове, что может быть и то, и то. А во второй части эту реакцию лучше не использовать. Но если что, то в побочных продуктах будет K₂MnO₄ и H₂O.
Жесткое окисление алкенов
Жесткое окисление протекает в присутствии кислого раствора KMnO₄ или K₂Cr₂O₇ при нагревании. В качестве среды лучше брать H₂SO₄, т.к. она не будет взаимодействовать с алкеном.
Нужно запомнить 3 варианта окисления. Общий принцип такой: при жестком окислении двойная связь разрывается, а углероды при двойной связи окисляются в -COOH (если углерод связан с другими углеродами) или в CO₂ (если углерод не связан с другими углеродами).
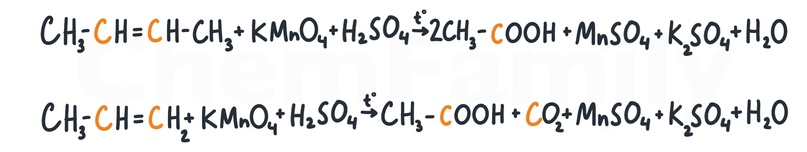
Еще одним вариантом является жесткое окисление метилпропена. Двойная связь так же рвется, образуется CO₂ (логично) и ацетон. Второй углерод окисляется не в кислотную группу -COOH, а в кето-группу -С(O)-. Это происходит из-за того, что группа -COOH не может располагаться в середине углеродного скелета, потому что имеет только 1 связь со скелетом молекулы (смотри на черточку рядом с COOH).
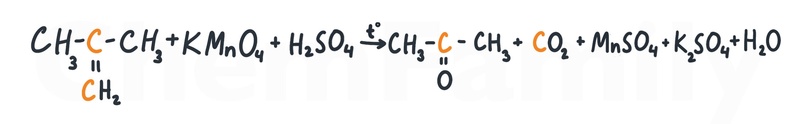
Если в качестве окислителя брать подкисленный серной кислотой раствор K₂Cr₂O₇, то получится то же самое, только в побочных продуктах вместо MnSO₄ будет Cr₂(SO₄)₃.
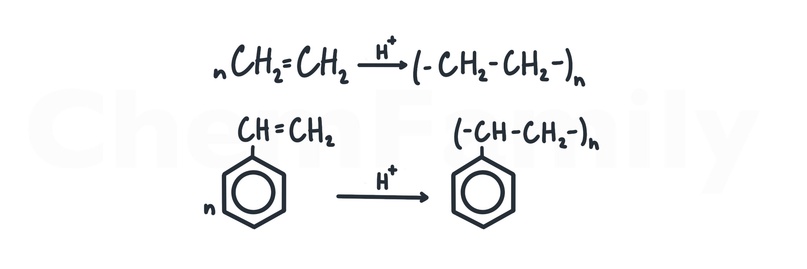
Полимеризация алкенов
Эта реакция во 2 части не встречается, поэтому можно в качестве катализатора запомнить просто H⁺.
Дегидрогалогенирование галогеналканов
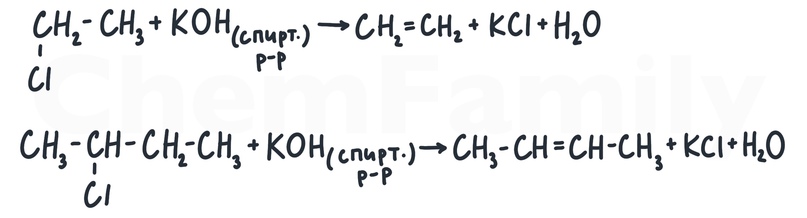
Для дегидрогалогенирования, отщепления галогена и водорода, используется спиртовой раствор щелочи, это важно указывать!
При дегидрогалогенировании несимметричных галогеналканов водород отнимается от того углерода, где водородов меньше (правило Зайцева).
Дегидратация спиртов
В этих реакциях очень важно точно указывать температуру, посколько при разной температуре получаются разные продукты.
При температуре <140⁰С идет межмолекулярная дегидратация, и образуется простой эфир. При температуре >140⁰С идет внутримолекулярная дегидратация, и образуется алкен. Во второй части важно писать конкретную температуру, а не больше-меньше. Лучше сразу запомнить 180⁰С и 120⁰С.
При дегидратации несимметричных спиртов водород отнимается по правилу Зайцева — водород отнимается от того углерода, у которого меньше водородов.
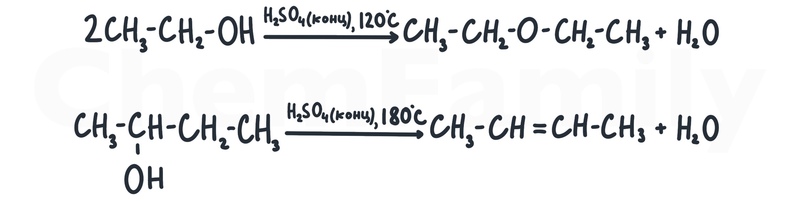
Получившийся простой эфир называется диэтиловым (или этоксиэтаном).
Дегалогенирование дигалогеналканов
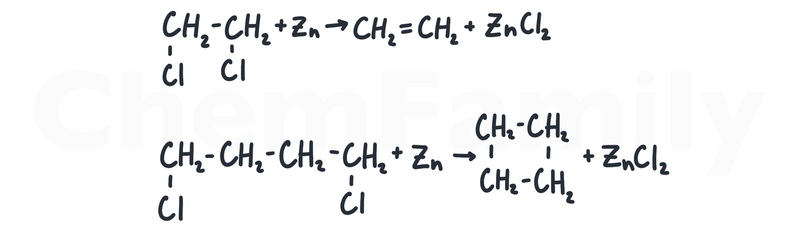
Если галогены расположены рядом, то образуется алкен. Если галогены расположены по краям молекулы, то образуется циклоалкан.
Вместо Zn можно использовать Mg.
неФИПИшные реакции
Дальше идут реакции, которые в ЕГЭ не попадались (неФИПИшные), но попадались в разных авторских сборниках для подготовки. Их можно выучить, но не в первую очередь. И во второй части я бы их не писал, если есть аналогичные ФИПИшные реакции.
Получение эпоксидов
Окисление алкена кислородом в присутствии нагретого до 200⁰С серебра приводит к образованию эпоксида.
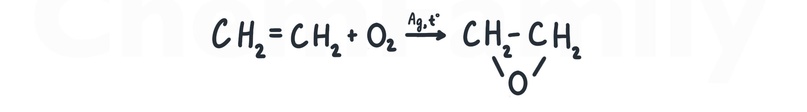
Окисление до альдегидов
Алкены с концевой двойной связью окисляются в присутствии CuCl₂ и PdCl₂ до альдегидов.

