- Умный справочник
- Физика
- Молекулярная физика. Начало.
Молекулярная физика. Начало.
Ну что, опустимся с тобой почти на самое дно (не путать с днищем), а почти, потому что есть еще глубже. А мы разберемся с молекулами вещества. Название — молекулярная физика на это слегка намекает.
Этот раздел весьма простой, когда речь идет о твердых телах и жидкостях, и не менее сложный в газах. Обо всем по порядку.
Простое начало
То, что подходит для твердых, подходит и газам. Начнем с количества вещества. Молекул очень много, так что выражать их просто числами не удобно, тогда один хороший человек по фамилии Зорро Авогадро решил огромную кучу молекул взять за такую величину как моль. И теперь удобство не знает границ, ведь 6,02*10^23 (это, кстати, число Авогадро) столько молекул составляют 1 моль вещества.
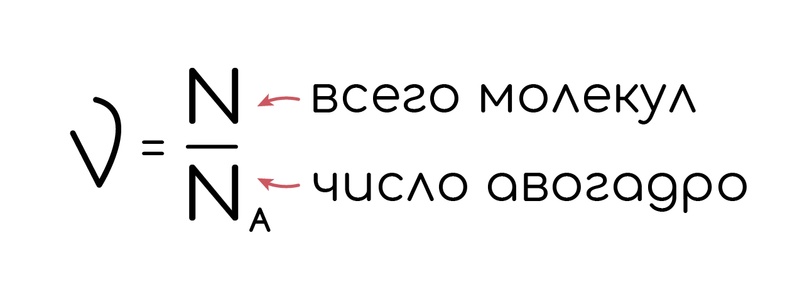
Молекулы разных веществ имеют разную массу, об этом позаботился Менделеев, в своей таблице, обозначив в ней, сколько весит один моль каждого вещества (молярная масса), и количество ню теперь можно найти и вот так:
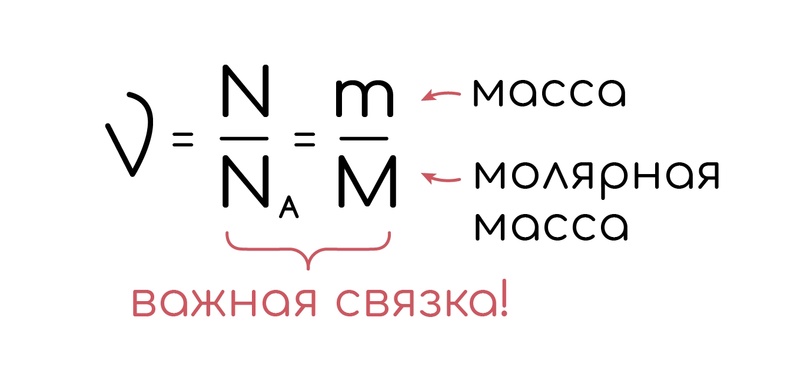
Связка, кстати, очень важная, запомни ее, она объединяет частые величины.
Иногда необходимо знать массу молекулы, и найти ее проще некуда, нужно просто поделить общую массу на их количество:
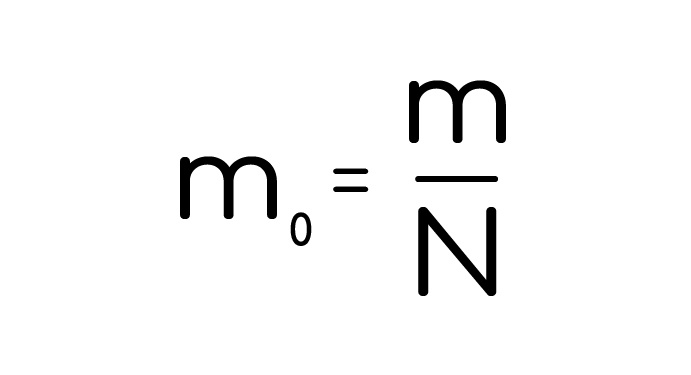
Когда возникает необходимость знать концентрацию молекул, то есть их количество на единицу объема, а необходимость возникает, так как концентрация постоянна вне зависимости от объема вещества. И находится она по формуле:

Газы
А вот теперь то, что в больше части относится к газам. Во первых рассматривать мы будем идеальные газы, это те, молекулы которых не взаимодействуют и представляются нам как упругие шарики.
Начнем со скорости их движения. Так как молекулы немного меньше бильярдных шаров, наблюдать за ними сложно и есть несколько скоростей, в зависимости от близости к реальным значениям. Это средняя арифметическая, наиболее вероятная и средняя квадратичная. Остановимся на последней, так как именно она встречается на ЕГЭ и находится по формуле:
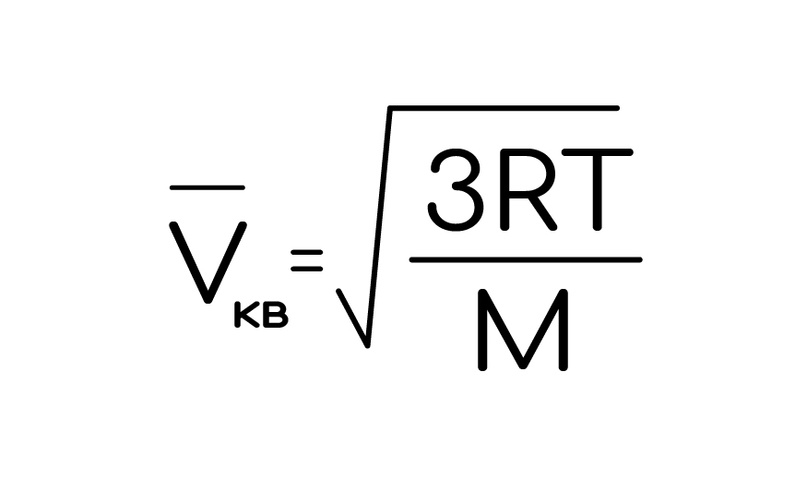
Полоска сверху значит, что величина средняя, R – универсальная газовая постоянная, это константа 8,31, размерность, честно говоря, значения не имеет, T – температура в Кельвинах, тут уже только система Си. А чтобы перевести в шкалу Кельвина, напоминаю, надо прибавить к Цельсия 273 градуса.
Давление Газа
Это большой вопрос, который пронизывает всю молекулярку и много формул, по которым оно находится. Я бы рекомендовал запомнить следующие:
Кинетическая энергия молекул, кстати, находится также, как и в механике. Еще есть простая формула для этой энергии E=1.5kT, ее тоже стоит запомнить. А постоянная Больцмана во-первых, как и все остальные константы, дается в справочных материалах, а во-вторых, для справки, находится:
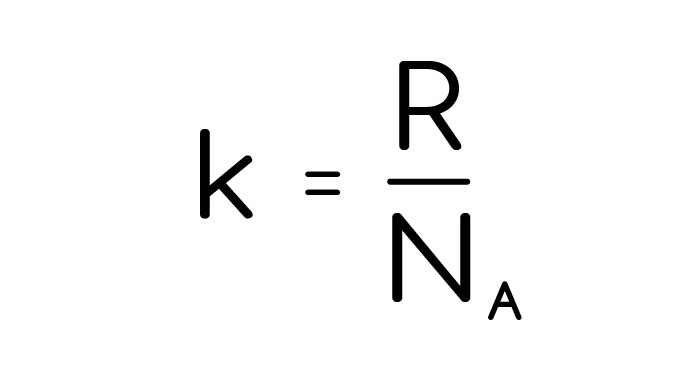
Есть еще некоторые формулы, но их я дам в конце. А сейчас Закон дальтона.
Закон дальтона не очень часто используется на ЕГЭ, но он там есть и надо быть готовым ко всему. Он говорит о том, что общее давление смеси газов в сосуде складывается из давлений каждого газа отдельно.

Казалось бы, простая вещь, но забывать про нее совсем не стоит.
Почему, собственно, я так насторожен по поводу газа? Жидкость практически несжимаема, твердые тела тоже, хотя не всегда, имеют определенный объем и ведут себя так, как нам хочется. А вот газы не имеют ни формы, ни объема, сколько им дадут, они займут всё. От таких характеристик, как давление, температура и объем зависит и плотность газа. Эта изменчивость усложняет все расчеты, связанные с ним.
И обещанные формулы для массы молекулы и давления газа. Я не настаиваю на том, чтобы ты их учил, ведь они без проблем выводятся из всех формул, которые мы писали выше, но посмотреть на них не повредит:
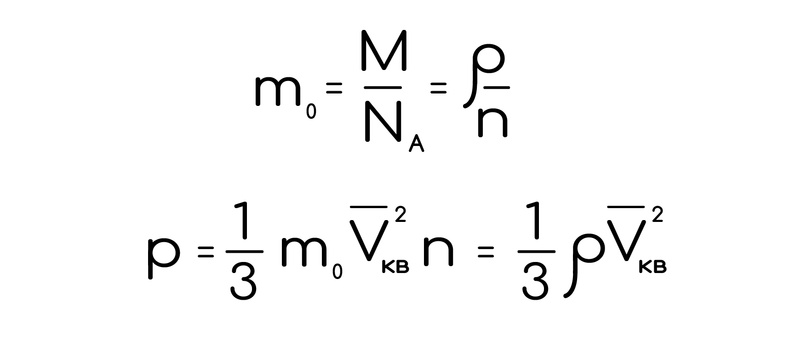
А мы встретимся в следующей статье, на самой важной теме всей молекулярки, на которую дается большинство задач в ЕГЭ – уравнении Менделеева-Клапейрона.
